МОДЕЛЬ БОРА
 Боровская модель атома — полуклассическая модель атома, предложенная Нильсом Бором в 1913г.
Боровская модель атома — полуклассическая модель атома, предложенная Нильсом Бором в 1913г.
За основу он взял планетарную модель атома, выдвинутую Эрнестом Резерфордом.
Радиус первой орбиты в атоме водорода R0=5,2917720859(36)⋅10−11 м, ныне называется боровским радиусом, либо атомной единицей длины и широко используется в современной физике. Энергия первой орбиты E0=−13.6 эВ представляет собой энергию ионизации атома водорода.
Энергия ионизации — разновидность энергии связи или, как её иногда называют, первый ионизационный потенциал, представляет собой наименьшую энергию, необходимую для удаления электрона от свободного атома в его низшем энергетическом (основном) состоянии на бесконечность.
Реально электрон может приблизится к протону на расстояние значительно меньше боровского радиуса или даже на него упасть (нейтрон) — это не противоречит законам физики.
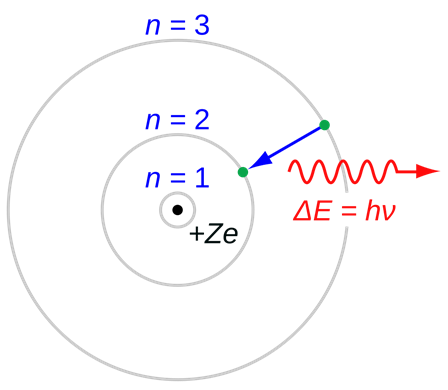
При этом с точки зрения классической электродинамики, электрон в модели Резерфорда, двигаясь вокруг ядра, должен был бы излучать энергию непрерывно и очень быстро и, потеряв её, упасть на ядро. Чтобы преодолеть эту проблему, Бор ввёл допущение, суть которого заключается в том, что электроны в атоме могут двигаться только по определённым (стационарным) орбитам, находясь на которых они не излучают энергию, а излучение или поглощение происходит только в момент перехода с одной орбиты на другую. Причём, стационарными являются лишь те орбиты, при движении по которым момент количества движения (момент импульса) электрона равен целому числу постоянных Планка